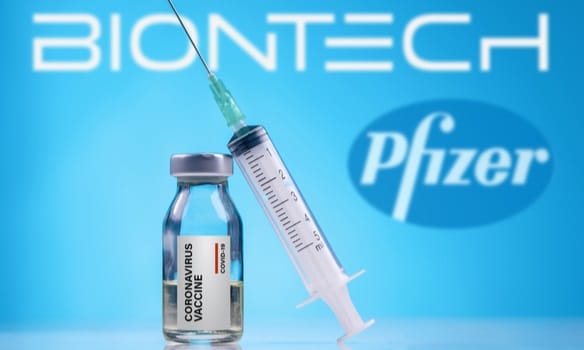
Днес Американската администрация по храните и лекарствата (FDA) промени разрешението за спешна употреба (EUA) за Pfizer-BioNTech Ваксина срещу COVID-19 за:
- Разширете употребата на единична бустер доза, за да включите употреба при лица на възраст от 12 до 15 години.
- Съкратете времето между завършването на първичната ваксинация на ваксината Pfizer-BioNTech COVID-19 и бустер дозата до най-малко пет месеца.
- Разрешете трета първична серия доза за определени имунокомпрометирани деца на възраст от 5 до 11 години.
„По време на пандемията, тъй като вирусът, който причинява COVID-19, непрекъснато се развива, необходимостта FDA да се адаптира бързо означава използването на най-добрата налична наука за вземане на информирани решения с мисъл за здравето и безопасността на американската общественост“, каза Действащ FDA Комисар Джанет Уудкок, д-р
„С настоящата вълна от варианта на омикрон е изключително важно да продължим да предприемаме ефективни, животоспасяващи превантивни мерки като първична ваксинация и бустери, носене на маски и социално дистанциране, за да се борим ефективно с COVID-19.
Какво трябва да знаете:
Бустерите вече са разрешени за хора на 12 и повече години
Днешното действие разширява използването на единична бустер доза от Pfizer-BioNTech Ваксина срещу COVID-19 да включва употребата й при лица на възраст до 12 години.
- Агенцията е определила, че защитните ползи за здравето от единична бустер доза на ваксината Pfizer-BioNTech COVID-19 за осигуряване на продължителна защита срещу COVID-19 и свързаните с тях сериозни последици, които могат да възникнат, включително хоспитализация и смърт, надвишават потенциалните рискове за индивидите От 12 до 15 години.
- - FDA прегледа реални данни от Израел, включително данни за безопасност от повече от 6,300 лица на възраст от 12 до 15 години, които са получили бустер доза от ваксината най-малко 5 месеца след завършване на първичната серия за ваксинация с две дози.
- Тези допълнителни данни позволиха на FDA да преоцени ползите и рисковете от употребата на бустер при по-младата юношеска популация в условията на текущия скок на случаите на COVID-19.
- Данните показват, че няма нови опасения за безопасността след бустер в тази популация. До момента няма съобщени нови случаи на миокардит или перикардит при тези лица.
КАКВО ДА ОТНЕМЕ ОТ ТАЗИ СТАТИЯ:
- Агенцията е определила, че защитните ползи за здравето от единична бустер доза на ваксината Pfizer-BioNTech COVID-19 за осигуряване на продължителна защита срещу COVID-19 и свързаните с тях сериозни последици, които могат да възникнат, включително хоспитализация и смърт, надвишават потенциалните рискове за индивидите От 12 до 15 години.
- Тези допълнителни данни позволиха на FDA да преоцени ползите и рисковете от употребата на бустер при по-младата юношеска популация в условията на текущия скок на случаите на COVID-19.
- Today’s action expands the use of a single booster dose of the Pfizer-BioNTech COVID-19 Vaccine to include its use in individuals as young as 12 years of age.